在多數細胞中,水分子可以透過簡單的滲透機制緩慢通過細胞膜之磷脂雙分子層(Phospholipid Bilayer),但科學家卻發現在一些上皮細胞於滲透壓梯度存在時,其水分子之滲透性遠高於一般擴散現象。因此,水分子係透過特殊轉移機制跨越細胞膜的概念被提出,爾後更進一步衍生出特定的膜蛋白具有引導水分子傳輸之理論。直到1992年,Johns Hopkins University的Peter Agre發現了第一個水通道蛋白(Aquaporin-1; AQP1),當時又稱CHIP 28,證實高水分子滲透性膜蛋白的存在,開始了AQP研究的新領域。此外,Peter Agre與Roderick MacKinnon更是共同榮獲了2003年的諾貝爾化學獎。
水通道蛋白(Aquaporin; AQP),又稱水通道(Water Channel),其於細胞膜上組成特殊的孔道,可控制水分子在細胞的進出,為專屬水分子跨越細胞膜的「快速通道」(圖一)。隨著分子工程和高解析分析技術的進展,對水通道蛋白的研究亦提供了分離膜材在水處理之應用上新的思路,透過水通道概念的導入,使得膜材可以在保留既有之脫鹽(Desalination)功能下,進一步獲得更為突出的產水量。因此,近年來水處理仿生膜(Biomimetic Membrane)的相關研究已逐漸開始興起。
水通道蛋白與水的滲透
目前,水通道蛋白之分子結構相關研究的原型通常來自於AQP1,係因AQP1的分子結構最為分明,它在細胞膜中主要以四聚體的形式存在(圖二),而在四個單體的中空部分皆具有獨立的水通道,每一個孔道的大小僅能容納一個水分子通過,直徑約3.8 Å。AQP1的單體結構是一條含有6個螺旋的單肽鏈,而這6個螺旋肽鏈荷則互相纏繞構成一個不等邊的四邊形,其中,水通道孔道的形成與2個貫通細胞膜的螺旋肽鏈有關,該螺旋則是由多種胺基酸之串連序列組成。
水通道蛋白的水分子分離選擇特性目前認為有三個主要的機制,以下以AQP1來說明(圖三):①AQP1的中心通道呈啞鈴形狀,狹窄的部分對大多數孔徑較大的水合離子具有尺寸排除的作用;②進入水通道最狹窄的區域前,會經過一具電性選擇的篩選區域,該區域主要由精氨酸殘基所組成,對正電離子具有靜電排斥的作用;③在水通道的中點,存在兩個帶正電的偶極子,它會破壞氫鍵並阻礙質子通過,同時,偶極力會促進水分子重新排列,使其快速通過水通道。綜合而言,水分子在AQP通道中的快速轉運行為,則可以理解為水分子幾近是以「無摩擦」流(Frictionless Flow)的方式平滑地通過狹窄的疏水性通道。
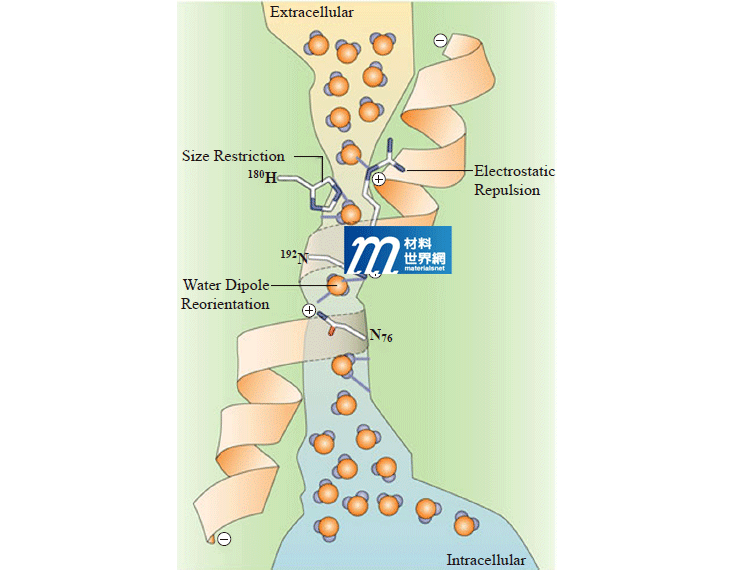
圖三、水通道蛋白分離選擇機制
水通道蛋白仿生膜
水通道蛋白仿生膜必須能滿足連續操作和功能穩定的條件,才具有應用於實際水處理程序的價值,故理想的水通道蛋白仿生膜應該具有以下特色:①高度可滲透性;②高選擇性;③高機械穩定度,能夠承受應用所需的壓力;④高化學和生物穩定度;⑤合理的成本進行規模化。目前,針對AQP的導入方式,水通道蛋白仿生膜的結構設計主要可分為兩種:①雙分子層支撐承載法(Supported Membrane Layers; SML):係以磷脂雙分子層或嵌段共聚物(Block Copolymer)作為AQP之載體,並形成一超薄之水通道層後,將其結合至高分子膜材上;②囊泡嵌入法(Vesicle Encapsulated Membranes; VEM):將含有AQP的囊泡導入至高分子膜材製程,接著透過界面聚合(Interfacial Polymerization)等方式將其固定至膜材之選擇層中(圖四)。
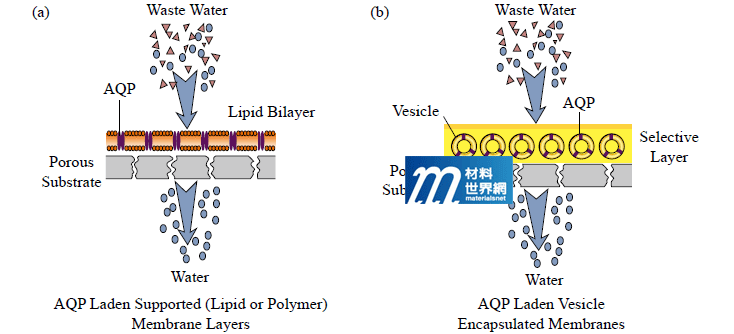
圖四、(a)SML;(b)VEM兩種不同結構設計之AQP仿生膜
水通道蛋白仿生膜之脫鹽應用
近年來,AQP仿生膜的開發已是薄膜脫鹽技術中重要的一環,係因透過水通道蛋白建構之膜材具有高水分子滲透性與選擇性的潛力,相關研究更指出,AQP仿生膜的膜材水滲透率(~600 LMH/bar)高於現今商售RO膜2個數量級,顯示…以上為部分節錄資料,完整內容請見下方附檔。
作者:顏嘉亨、黃盟舜、洪仁陽、梁德明 / 工研院材化所
★本文節錄自「工業材料雜誌」367期,更多資料請見下方附檔。